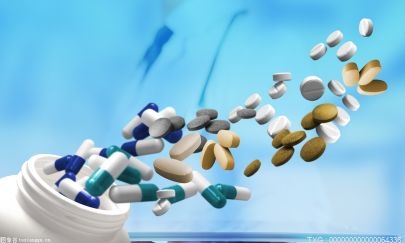
1月7日在美国巴尔的摩的马里兰大学医学中心拍摄的移植手术现场。 新华社发
当你的心脏即将停止跳动,如果有一个机会可重获“心”生,哪怕是一颗猪的心脏,你会接受吗?为了活下去,57岁的美国男子戴维·贝内特选择了接受。
人类从未停止对生命的探索,也不会拘泥于自然所赋予的躯体本身。今年1月份,全球首例猪心脏移植人体手术,无疑给器官移植技术带来了更宽广的发展空间,也给生命科学带来了更多的希望与思考。
这场特殊的心脏移植背后有怎样的科技突破?为什么会选择猪心脏移植?当前心脏移植面临哪些难题?当心脏因疾病即将停止跳动的时候,我们还有更多的选择吗?
一次大胆的尝试
戴维·贝内特患有心力衰竭,病情已进入终末期,不靠机器就无法维持正常的心肺功能。用他自己的话说:“要么死,要么移植。”
手术前,这名男子的心脏已无法为全身泵出足够的血液,仅靠一台ECMO(俗称“人工心肺机”)维系生命。也正因如此,贝内特已完全离不开病床,这样的日子过了大约50天。医生清楚,他的生命已进入倒计时。
根据报道,由于心力衰竭与心律不齐等病症的严重程度,贝内特已失去接受常规人体器官移植手术的资格。对他来说,如果想活下去,唯一的选择就是接受马里兰大学的实验性疗法,也就是这次的猪心脏移植。
河北省医科大学第二医院心脏外科主任陈子英说,心脏移植从手术技术上来说,基本已没有任何难度,手术成功率在95%以上,手术后一年的存活率高达94%-95%。
我国的第一例、同时也是亚洲首例心脏移植手术是1978年在瑞金医院完成的,此后,心脏移植在中国不断开展,也有移植后患者存活20年以上的报道。
但是,医学界还面临着一大难题:心脏从哪里来?
“器官移植分为异种移植、同种异体移植和亲体移植。”陈子英介绍,其中,亲体移植是指有血缘关系的亲人之间的器官移植;同种异体移植指器官的供者和受者同种但非同一个体,遗传基因有差异,常伴排斥反应;异种移植,即跨物种器官移植。当前国内90%以上的器官移植都是同种异体移植。
为了解决移植器官短缺的困境,科学家们将视线转向了动物器官。
其实,有关猪的异种器官移植,科研人员早在多年前就已经开始研究。目前,猪的心脏瓣膜、眼角膜等组织工程产品已广泛应用于人体临床,猪胰岛细胞和皮肤异种移植已进入人体临床试验阶段,而猪的肾脏这种大器官的异种移植也已完成临床前试验,具备开展人体临床试验的基础。
这也不是一次空穴来风的“改造”猪心计划。为提高手术成功率,这次手术前,科学家团队已尝试将猪的心脏移植到50只狒狒体内进行试验,以研究免疫抑制、低血压、血液凝固受阻等术后反应的应对方法。而在猪心脏移植前,美国研究人员也成功将基因修改后的猪肾脏移植到了一位肾功能不全的脑死亡患者的大腿上,虽然体外观察试验只持续了三天,但没有出现排异反应。
从专业角度,专家们更关注的是患者移植手术之后的预后问题。
“当被基因编辑过的猪心脏移植到人的体内后,这位患者依旧有重重难关需要闯。”陈子英说,首先是术后恢复关,虽然媒体报道目前患者已脱离ECMO并开始下地走路,但未来情况如何尚不可知;其次,虽然目前患者没有出现急性器官排异反应,但此后会不会出现排异反应或慢性排异反应仍是未知数;此外,移植手术后人的抵抗力和免疫力较低,此时人体是否会出现感染,也是需要挺过的一关。一切,都需要时间来验证。
一颗基因编辑过的心脏
任何一次器官移植手术之后,排异反应都是术后最大挑战。
当人的机体察觉到外来器官时,抗原、淋巴细胞会首先作出反应,产生抗体。陈子英说,即使手术成功,患者也必须终身服用抗排药物。
当一颗没有被基因编辑过的猪心脏被移植到人的体内后,人体会迅速出现超急性免疫排异反应,结果可想而知。
猪携带有可能导致人类感染的病原体,包括弯曲杆菌、伤寒沙门氏菌、鼠疫杆菌等细菌,也包括圆环病毒、猪巨细胞病毒、猪逆转录病毒等病毒。
“针对移植器官的生物安全性问题,目前可利用屏障环境,结合剖宫产手术对供体猪进行净化。此外,还可以利用基因编辑技术去除猪内源性病毒。”陈子英说。
2017年,美国哈佛大学杨璐菡教授和她的团队通过内源性基因编辑方法,利用基因剪刀技术完成了猪内源性逆转录病毒相关酶基因的敲除,并成功克隆出无内源性病毒的“猪2.0”。
此次手术的关键点,也在于那颗被基因编辑过的猪心脏。
“科学家们利用一种细菌酶在哺乳动物细胞内剪辑基因,猪心脏的生长激素受体基因被敲除和灭活后,可以防止移植后的猪心脏在人体内继续生长。而且猪心脏内导致人类出现超急性排斥反应的三个基因也被敲除,以保证移植顺利进行。”专家介绍。
此外,还有六个人类抗排斥反应的基因被插入到了供体猪的基因组中,以使人体免疫系统更能耐受猪的心脏。
人类属于灵长类动物,与灵长类其他动物在生理解剖和新陈代谢等方面相似。因此,许多人不解,此次移植手术,为什么不选择移植猴子或狒狒的器官,而是选择猪的器官呢?
有专家介绍,灵长类动物曾被认为是异种器官移植理想的供体。但灵长类动物培育时间长,繁殖率低,饲养成本也较高,个体比人小,很难满足人类器官移植的需求。而且,非人灵长类动物危险性很大,它们自带的一些病毒如SIV(猴免疫缺陷病毒)、埃博拉病毒很容易传染给人类,当它们的器官移植到人体上发生重组之后,甚至会产生更多有害病毒。
“猪是异种器官供体的最佳选择对象在国际上已成为共识。”陈子英说,猪的基因、结构与人类有许多相似之处。猪的心脏与人的心脏大小差不多,其管道分布和动力输出也相类似。再加上猪产仔多,生长快,成本低,所以被认为是最佳供体物种。
“尽管异种器官移植研究取得了很大进展,但移植器官的功能兼容性问题却成了尚待解决的技术挑战,被移植的猪器官能否完全发挥原有人体器官维持荷尔蒙分泌、代谢平衡等功能仍有待检验。”杨璐菡公开表示,解决供体猪的异种病毒传播风险和免疫兼容性只是“万里长征第一步”,目前还需要不停地摸索和改进异种移植器官在功能上的兼容性。
据了解,目前,异种器官移植仍处于前沿科技赛道,世界上只有美国、德国、中国、日本等几个少数国家开展研究,大部分是以实验室的方式进行,少量以企业的方式进行研究。在我国,异种移植研究正处于临床前阶段,部分医院及研究机构、公司已经展开布局,将猪的大型器官移植进猴子体内的试验已经开展多年。国内目前已有数家致力于研发异种器官移植的公司。开展临床试验是实现技术超车的关键。
如何才能延续生命的希望
数据显示,当前中国大约有1200万心衰病人,其中有5%左右为重症心衰患者。而随着心血管疾病的年轻化,全球心衰患者呈逐年上升的趋势。对很多人来说,心脏移植是他们活下去的唯一希望。
陈子英介绍,虽然移植手术的成功率很高,但每年接受心脏移植手术的患者只有500人-600人。“心脏移植供体紧缺是限制心脏移植的最重要因素。遗憾的是,相对于肝脏和肾脏来说,受心脏器官的特殊功能和地域风俗影响,心脏的器官供体较少。供体要求更加严格。”
心脏供体有怎样的标准呢?
陈子英介绍,这颗心脏必须是一颗年纪在60岁以下的心脏,最好在50岁以下。而且,这颗心脏必须没有重大心脏疾病、没有传染病且不存在被感染的情况。此外,心脏的移植者和提供者的体重需要基本一致,差异须保持在20%以内,两人的血型和HLA抗原需要相配。
那么,在供体短缺的情况下,未来的心脏移植是否还有别的方案呢?
陈子英表示,人工心脏是治疗终末期或重症心力衰竭患者的有效手段,也是代替心脏移植的唯一有效治疗手段。从20世纪50年代开始,世界各国已开始研究“人工心脏”。从第一代仿生“人工心脏”到第二代功能性“人工心脏”,如今已跨越到第三代的全磁悬浮式“人工心脏”。
但在欧美日等发达国家,目前单台人工心脏的售价在10万美元左右,安装人工心脏存在不小的局限性。
此外,陈子英也提到,用患者自身的干细胞或胚胎细胞通过实验室培养制造出一颗与原始心脏“同根生”的心脏也是方法之一,但目前这项技术并不成熟,依旧存在于美好的愿景之中。
“这次‘猪心脏’移植手术是一个特例,并不意味着未来一大批心衰患者可以通过移植‘猪心脏’来挽救生命,真正运用到临床还很遥远。”很多专家都认为,即便等技术已经相当成熟,这样一颗不一样的心脏肯定不会便宜,治疗费用同样也是需要考虑到的现实问题。(河北日报记者王璐丹)